2023年8月31日,市场监管总局会同国家卫生健康委、国家中医药局制定并联合发布《允许保健食品声称的保健功能目录 非营养素补充剂(2023年版)》(以下简称《目录》)及配套文件。配套文件中正式提出对于已批准注册的产品中注册证书“无有效期和无产品技术要求”的产品(以下简称“双无”产品)展开换证工作。
2023年12月27日,市场监管总局发布公开征求《在产在售“双无”保健食品集中换证审查要点(征求意见稿)》(以下简称“意见稿”)意见的公告。2024年11月1日,市场监管总局发布《在产在售“无有效期和无产品技术要求”保健食品集中换证审查要点》(以下简称《换证审查要点》)。
食品伙伴网总结了《换证审查要点》相比“意见稿”的主要变化,梳理了企业根据《换证审查要点》开展“双无”产品换证的工作要点,以供参考。
一、《换证审查要点》相比“意见稿”的主要变化
(一)省级局提出的换证意见
《换证审查要点》规定核发生产许可的省级局提出的换证意见由其报送市场监管总局,并抄送注册人,不采用“意见稿”拟由注册人向市场监管总局提交省级局出具的换证意见的建议;
删除了注册人对省级局意见所附产品技术要求进行修订时的资料要求,表明申请人不能对省级局意见所附产品技术要求进行修订;
删除了“意见稿”中要求省级局出具注册人主体资质情况确认意见的规定。
(二)申请人主体资质相关
《换证审查要点》删除了“意见稿”对于注册人处于注销、吊销、列入经营异常名录或违法失信企业名单等异常情形的,暂停受理的规定;
增加了原注册人有多个主体但部分主体注销时,存续注册人在换证时应提交的产品注册证书归属权声明或涉及的权利义务无争议承诺书及说明等资料要求。
(三)原料相关
对于原料用量或原料种类个数等超出现行规定的情况,《换证审查要点》增加了依据产品长期食用的安全性论证报告,经评估需要降低原料用量的,在收到不予批准换证意见后,重新进行换证申请时,可免于提供拟降低原料用量后产品的安全性评价试验材料,但需提供保健功能评价材料和卫生学、稳定性、功效成分/标志性成分检测等试验报告,论证产品保健功能与质量可控性的规定。
对于按照现行规定调整产品配方(含替换或去除原料)的,《换证审查要点》增加了按照现行新产品注册要求提交产品配方、生产工艺、标签说明书样稿、产品技术要求等研发资料的要求。
二、按照《换证审查要点》进行“双无”产品换证时的工作要点
(一)换证范围
过渡期(2023年8月31日起5年内)内在产在售的国产和进口“双无”产品。
(二)换证程序
1、注册人向市场监管总局提出变更申请
注册人按照《换证核查要点》的规定准备换证资料,并向市场监管总局提出变更申请,变更注册类别为“双无”换证。
2、省级局出具换证意见
省级市场监管部门根据产品实际生产的技术要求和监管情况,依据现行法律法规提出产品换证意见,报送市场监管总局,并抄送注册人。
3、技术审评
审评机构(市场监管总局食品审评中心)按照现行法律法规标准及有关规定开展换证审评,并将审评结论报送市场监管总局审批。
4、行政审批
符合要求的,换发新的注册证书,注册号更新为“国食健注G/J年代号+序号”(其中“年代号+序号”不变),证书备注栏标注原产品名称、原产品注册号及“原注册证书换证后失效”。
不符合要求的,不予批准换证申请。注册人可依据规定要求重新提出换证申请。
换发的注册证书或不予注册决定书,同时抄送注册人所在地和核发生产许可的省级市场监管部门。
(三)工作要点
1、申请人主体资质
换证申请人应当为注册人。进口产品的注册人为境外生产厂商。
2、换证意见出具单位
“双无”产品换证意见由核发生产许可的省级市场监管部门出具,即产品实际生产企业所在地的省级局,而不是注册人所在地的省级局。
3、产品名称
产品名称应当符合现行有关规定。保留产品原名称的,理由应当充分合理。产品名称的现行有关规定指:《保健食品命名指南(2019年版)》第四部分第(二)条第5款,“已获得批准证书的保健食品,其产品名称除不符合本条款规定外,符合本指南其他相关规定的,申请人可提出充分合理的理由申请保留原产品名称”。
调整产品名称的,可在新的产品名称后括号内标注产品原名称,使用至本次换发证书有效期结束。
4、进口“双无”产品换证
对于在产在售“双无”进口产品,相关材料符合《换证核查要点》规定的,注册人按照要求直接提出换证申请。相比国产“双无”产品换证提交的资料,还应当提交委托书、境外生产厂商的资质证明文件、生产企业质量管理体系证明文件、上市销售的证明文件、境外销售或进口销售的最小销售包装实样、注册人(境外生产厂商)在我国出入境检验检疫部门的备案或注册信息和产品进口信息。
5、换证涉及检测的要求
小结:
《换证核查要点》旨在集中规范在产在售“双无”产品注册证书,设立注册证书有效期,规范保健功能声称,完善产品标签说明书样稿、产品技术要求和产品档案信息,换发保健食品注册证书,实现保健食品注册与生产许可、监督管理衔接,落实落细生产企业主体责任和属地监管部门监管责任。
《换证核查要点》的发布意味着“双无”产品换证的正式开始,其详细规定了“双无”产品换证的流程及变更申请资料要求,对相关企业具有明确的指示作用,有利于整个行业的规范及可持续发展。
以上是食品伙伴网对《换证核查要点》的梳理和总结,食品伙伴网将对保健食品及其他特殊食品相关的法规进行持续性的更新与解读,敬请期待。
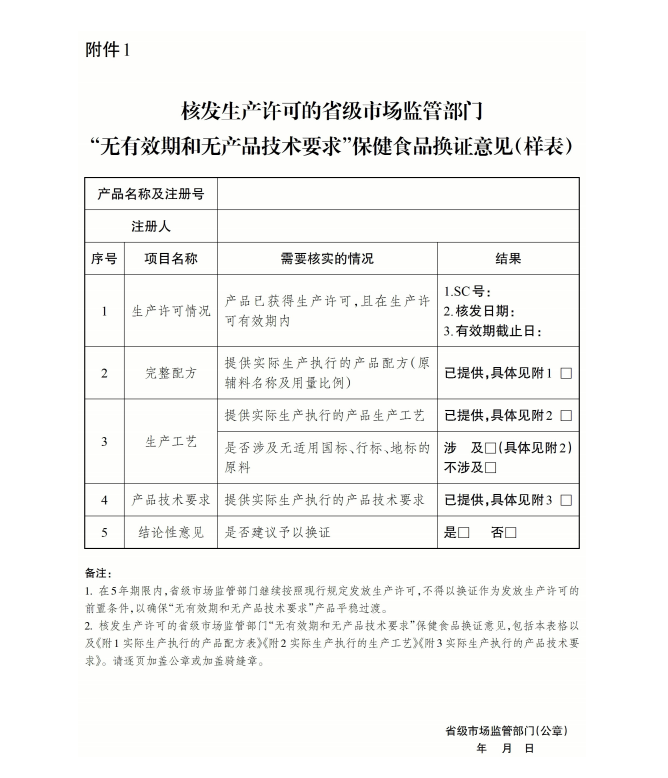
附件:
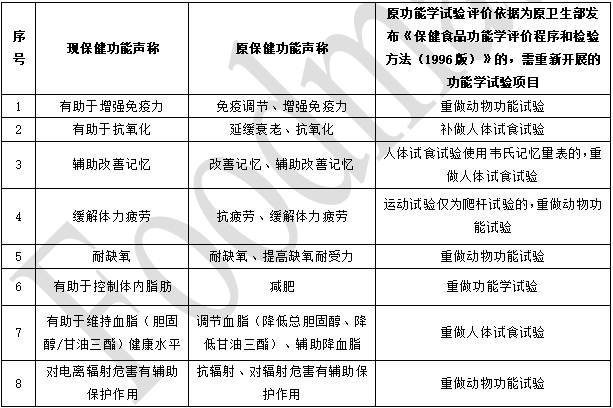
原功能学试验评价依据为原卫生部发布《保健食品功能学评价程序和检验方法(1996 版)》的8种功能的新旧保健功能声称对应关系和功能评价衔接要求。
附件:
《在产在售“无有效期和无产品技术要求”保健食品集中换证审查要点》已经2024年10月28日市场监管总局第27次局务会议通过, 现予公告, 自发布之日起施行。
市场监管总局
2024年10月30日